고가의 전해액 사용량 대폭 감소시켜, 에너지 밀도 향상과 가격 절감 기대
KAIST 김희탁 교수 연구팀, 차세대 전지 전해액 설계기술 개발
 |
| (왼쪽부터)김희탁 교수, 정진관 박사과정 |
최근, 드론 및 전기자동차 등 이동체의 항속거리 증대를 위해, 리튬이온전지의 용량 및 에너지 밀도의 한계를 극복할 차세대 전지로서, 리튬 황 전지가 주목을 받고 있다. 리튬 황 전지는 이론용량이 리튬이온전지 양극활물질 대비 9배의 이론용량을 가지는 황과 리튬이온전지 음극 활물질 대비 11배의 이론용량을 가지는 리튬금속을 활물질로 사용하여 높은 무게당 에너지 밀도가 가능한 이차전지이다. 또한, 지구상에 풍부한 황을 활물질로 이용하여, 전지 가격 저감에 유리하다는 장점을 가지고 있다.
그러나 리튬 황 전지는 부도체인 황의 느린 전기화학 반응속도 문제를 극복해야 하고, 리튬금속 음극의 전해액 분해반응을 억제해야 하는 과제를 안고 있다. 최근 10여 년간 리튬 황 전지에 관한 연구가 집중됐으나, 아직 고에너지밀도와 장수명을 동시에 구현하기 위해서는 여러 기술적 난제를 해결해야 한다.
국내 연구진이 리튬-황 전지를 경제적으로 설계하되 성능은 획기적으로 개선한 기술개발에 성공해 차세대 배터리 기술개발에 한 발 더 다가섰다.
KAIST(한국과학기술원)는 생명화학공학과 김희탁 교수팀이 기존 대비 전해액의 함량을 4배 이상 줄인 리튬-황 전지를 개발했다고 25일 밝혔다. 리튬-황 전지는 차세대 배터리 기술 중 연구개발이 가장 활발하게 이뤄지는 기술이다. 리튬-황 전지는 휴대용 전자기기와 전기자동차에 사용되는 리튬이온전지에 비해 에너지 밀도가 2~3배 높아서 이를 사용하면 전기동력 기체 무게를 크게 줄일 수 있기 때문이다.
리튬-황 전지는 가벼운 황과 리튬금속을 활물질(화학적으로 반응하여 전기에너지를 생산하는 물질)로 이용하기 때문에 중금속 기반인 리튬이온전지에 비해 경량화가 가능하다. 특히 지구에 풍부하게 존재하는 황을 활용해 저가의 전지를 구현할 수 있다는 점 때문에 산업계와 학계로부터 그동안 많은 주목을 받아왔다. 다만 리튬-황 전지는 리튬이온전지와 달리 매우 높은 전해액 함량을 갖고 있다. 전지 무게의 40%에 달하는 과량의 전해질 사용은 전지 무게 증가로 인해 그동안 리튬-황 전지의 고에너지밀도 구현에 큰 걸림돌이 돼왔다. 리튬-황 전지는 황이 방전되고 난 후의 산물인 `리튬 폴리 설파이드(Lithium poly sulfide)'가 전해액에 용해된 상태에서 빠른 충 ‧ 방전 특성을 갖는다.
이 전해액 양을 낮추면 리튬 폴리 설파이드의 용해량이 감소해 용량 및 출력이 저하되는 문제가 발생한다. 또 리튬금속 음극이 전해액을 분해해 전해액이 고갈되는 문제는 낮은 전해 액체량에서 더욱 심해져 결국 전지 수명을 떨어뜨린다.
김희탁 교수 연구팀은 이번 연구를 통해 리튬 나이트레이트 염과 같이 높은 전자공여(다른 화합물에 전자를 주는 성질) 능력이 있는 염을 전해질에 주입하면 폴리 설파이드의 용해도를 증가시킴과 동시에 리튬금속에서 전해질 분해를 억제할 수 있음을 규명했다. 리튬이온과 결합력이 강한 나이트레이트 음이온이 리튬이온의 `용매화 껍질(Solvation Shell)' 역할을 수행함으로써 리튬 폴리 설파이드의 해리도를 증가시켜 결과적으로 용해도가 향상된다는 사실도 증명했다. 아울러 용매화 껍질 구조변화가 전해액 용매 분자와 리튬금속과의 접촉을 낮춰 분해반응을 억제하는 현상도 확인했다.
김희탁 교수팀은 이번 연구를 통해 전해액 성분 중 리튬 염 물질 하나만을 교체하는 간단한 방법으로 에너지 밀도를 높이면서 고가의 전해액 사용량을 4배 이상 줄여 가격을 대폭 절감하는 성과를 거뒀다. 김희탁 교수는 "이번 연구는 황 양극과 리튬금속 음극의 성능을 동시에 높일 수 있는 전해액 설계원리를 제시했다는 점에서 의미가 크다ˮ면서 "차세대 전지 전해액 설계산업 전반에 걸쳐 넓게 응용되기를 기대한다ˮ고 말했다.
KAIST 생명화학공학과 석사졸업생인 추현원 학생(現 MIT 박사과정 재학 중)과 정진관 박사과정이 공동 제1 저자로 참여한 이번 연구결과는 국제 학술지 `어드밴스드 에너지 머티리얼즈(Advanced energy materials)' 6월 2일 字 표지논문으로 실렸다. (논문명: Unraveling the Dual Functionality of High-Donor-Number Anion in Lean-Electrolyte Lithium-Sulfur Batteries)
한편, 이번 연구는 LG화학, KAIST 나노융합연구소, 과학기술정보통신부 기후변화대응과제의 지원을 받아 수행됐다.
□ 연구 개요
에너지 밀도 향상을 위해서, 활물질인 황의 활용률을 높이거나 전해질의 함량을 감소시키는 연구가 이루어져 왔다. 그러나 전해액의 함량을 감소시키는 경우, 황의 활용률이 감소하게 되는 문제에 봉착하였다. 황의 중간방전 산물인 리튬 폴리 설파이드는 전해액에 해리되어 용해된 상태에서 빠르고 원활한 충 ‧ 방전을 일으킨다. 따라서 낮은 전해 액체량에서는 리튬 폴리 설파이드의 용해량이 감소하여 황 활용률이 떨어진다.
한편, 전지 사이클 수명향상을 위해서는, 리튬 황 전지에 사용되는 전해질이 리튬금속에 의해 분해되어 고갈되는 문제를 해결해야 한다. 이러한 전해액 고갈은 전해액 함량이 감소함에 따라 더욱 심화되어 수명특성이 악화된다.
따라서 전해 액체량을 감소시키기 위해서는 (희박 전해액 조건), 폴리 설파이드의 용해도 문제 (양극)와 전해액 고갈에 대한 문제 (음극)를 동시에 해결해야 한다.
본 연구에서는, 리튬 이온의 용매화 껍질 구조를 제어하여 폴리 설파이드의 용해도를 높이고 전해액 용매의 분해를 억제하여, 희박 전해액 조건 (전해 액체량이 낮은 조건)에서도 고성능 구동이 가능한 리튬 황 전지를 개발하였다.
본 기술의 특징은 전해액의 리튬염으로서 리튬 나이트레이트 염을 사용한 것이다. 나이트레이트 음이온은 전자공여특성이 커서 리튬 이온 주변에서 용매분자를 밀어내고 용매화 껍질에 참여하게 된다.
나이트레이트 음이온과 리튬이온과 강한 상호작용력에 의해 리튬폴리설파이드에서 리튬이온이 나이트레이트 음이온으로 이동하게 되어 리튬폴리설이드는 폴리설파이드 음이온이 되어 높은 용해도를 가질 수 있게 된다. 따라서 낮은 전해액 함량에서도 용해상태를 유지할 수 있어 원활한 충 ‧ 방전 반응이 일어날 수 있다.
리튬금속 음극 표면에서는 리튬이온의 용매화 껍질에 참여한 분자들이 주로 위치하게 되므로, 나이트레이트 음이온에 의해 껍질에서 밀려나간 용매분자의 분해반응 역시 감소하게 된다. 또한 나이트레이트 음이온은 리튬금속표면에 전해액 반응을 억제시키는 피막을 형성할 수 있어, 수명성능을 보다 향상시킨다.
이번 연구는, 전해액 음이온의 간단한 설계만으로 리튬 황 전지의 양극과 음극의 문제점을 동시에 해결할 수 있다는 점에서 기술적 의미가 높다고 하겠다.
□ 용어 설명
1. 리튬 황 전지 (Lithium Sulfur Battery)
리튬과 황을 활물질로 사용해서 기존의 리튬이온 배터리보다 이론용량이 4배 이상 높다는 장점이 있는 차세대 리튬 배터리임.
2. 전해질 (Electrolyte)
전지에 사용되는 이온 전도성을 가지는 액체. 주로 리튬 염과 극성유기용매로 구성됨
3. 전자공여도 (Donor Number)
용매 혹은 리튬 염이 전자가 부족한 분자 혹은 원자에게 전자를 공여하려고 하는 특성을 나타내는 지표.
4. 용매화 껍질 (Solvation Shell)
이온이 용매에 용해되는 경우, 이온과 상호작용력이 강한 용매 분자가 이온 주위에 선택적으로 위치하게 됨. 이러한 상호작용력에 의해 이온주위를 둘러싸고 있는 분자들에 의해 형성된 층을 용매화 껍질이라 일컬음.
□ 그림 설명
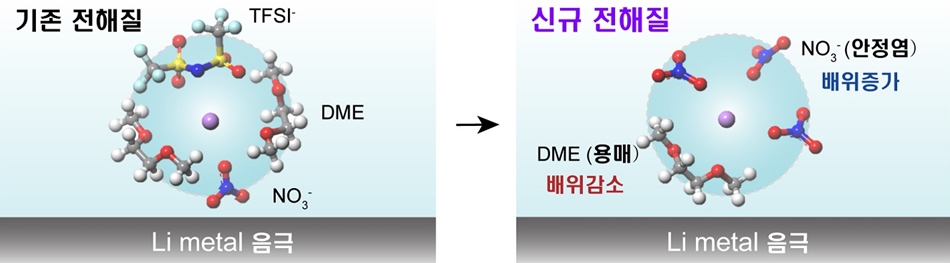 |
| 기존전해액과 개발전해액의 리튬 용매화 껍질 구조 차이 |
그림 1. 기존전해액과 개발전해액의 리튬 용매화 껍질 구조 차이. 개발전해액에는 나이트레이트 염이 용매 (DME)를 밀어내고 용매화 껍질에 참여함.
◇김희탁 교수 이력시항
1. 인적사항
○ 소속 : KAIST 생명화학공학과
2. 학력
1989-1993 학사, KAIST, 화학공학과
1993-1995 석사, KAIST, 화학공학과
1995-1999 박사, KAIST, 화학공학과
3. 경력사항
○ 1999-2001 고등기술원 책임연구원
○ 2001-2002 주)네스 수석연구원
○ 2003-2009 삼성SDI 책임연구원
○ 2009-2013 삼성SDI 수석연구원
○ 2013-현재 KAIST, 생명화학공학과, 부교수
○ 2016-현재 KAIST, 차세대이차전지인력양성센터 센터장
○ 2017-현재 KAIST, 나노융합연구소, 차세대배터리센터 센터장
 |
| (왼쪽부터)김희탁 교수, 정진관 박사과정 |
KAIST 홍보실 제공
노벨사이언스 science@nobelscience.co.kr